La maladie de Parkinson est un trouble qui progresse généralement au cours des années. Pour les patients au stade avancé de la maladie où les options de traitement ont déjà été limitées, de nouvelles thérapies ont émergé sur le marché au cours des dernières années.
Prof Dr Rejko Krüger, neurologue au Centre Hospitalier de Luxembourg et chercheur au Luxembourg Center for Systems Biomedicine à l'Université de Luxembourg, et des neurologues allemands avec lesquels il collabore ont publié le mois dernier, dans la revue scientifique ‘Journal of Neural Transmission’, un document de synthèse sur les thérapies existantes et les soins centrés pour les patients atteint de la maladie de Parkinson au stade avancé.
"La plupart des gens connaissent l’existence des comprimés de Lévodopa comme traitement pour la maladie de Parkinson. Mais il y a désormais beaucoup plus d'options disponibles, en particulier lorsque la L-DOPA ne présente plus l'effet désiré. « Dans cet article, nous voulions offrir un aperçu détaillé des options de traitement, en vertu de quels critères les patients peuvent être sélectionnés pour le traitement le plus approprié et le plus efficace, cela afin d’améliorer leur qualité de vie », explique le Prof. Dr. Rejko Krüger, le but de l'étude se concentre sur des traitements tels que l'application du Lévodopa dans l'intestin, l'application sous-cutanée de l'apomorphine et la stimulation cérébrale profonde.
Application de la lévodopa dans l'intestin
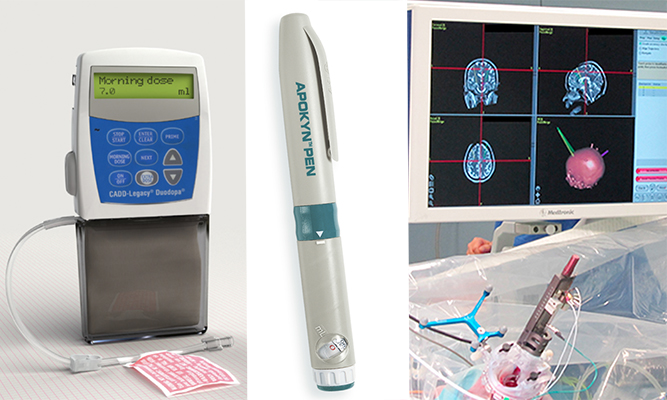
Les patients éprouvent des fluctuations motrices sous traitement avec des comprimés de lévodopa, principalement en raison du cheminement fluctuant de la substance jusqu’au cerveau. Par conséquent, le même composé peut être appliqué directement là où l'absorption a lieu, avec un gel (lévodopa-carbidopa gel intestinal (LCIG)) appliqué directement dans l'intestin grace à une pompe que l’on peut poser dans sa veste. Le lévodopa est continuellement absorbé, réduit les fluctuations motrices et peut également améliorer les symptômes ‘non moteurs’ comme le sommeil, la fatigue, la douleur, etc…Hors mis les complications qui pourraient survenir après une chirurgie-PEG ou avec l’appareil, le poids et les niveaux de vitamine B12 des patients doivent être soigneusement surveillés. "La thérapie de LCIG est recommandée pour les patients souffrant de maladie de Parkinson de façon avancée, et elle doit être administrée dès que les symptômes moteurs ne peuvent plus être contrôlés avec des comprimés", explique Krüger. «Généralement les patients s’adaptent rapidement au poids et à la taille de la pompe. L’administration de la perfusion s’établie en fonction des besoins des patients et demande quelques jours jusqu'à ce qu’une dose stable soit déterminée».
Apomorphine
L'apomorphine est un médicament connu depuis déjà longtemps pour le traitement de la maladie de Parkinson, mais son administration orale est apparue impossible en raison des fortes doses nécessaires et des effets secondaires se manifestants. Cependant, une seule injection d'apomorphine sous-cutanée ou une administration continue par le biais d’une pompe s’avère très efficace chez les patients parkinsoniens, car lorsque le médicament est administré par voie orale, des fluctuations motrices inefficaces se produisent. De "Simples injections d’Apomorphine via un stylo injectable sont considérées comme médicament de secours en cas de phases dites 'off' avec des troubles de mouvement. Pour les stades plus complexes de la maladie, la pompe apomorphine a prouvé son efficacité quant à la suppression des fluctuations motrices et l’amélioration de la qualité de vie des patients ", dit Krüger.
La stimulation cérébrale profonde
En raison de la perte des neurones dopaminergiques dans la substantia nigra, une certaine zone se trouvant au milieu du cerveau devient alors hyperactive cela favorisant ainsi les problèmes moteurs typiques de la maladie de Parkinson. Par conséquent, avec la stimulation cérébrale profonde (DBS) des électrodes peuvent être implantée chirurgicalement dans les zones hyperactives du cerveau et ainsi traiter les symptômes par des impulsions électriques calmant les neurones hyperactives. Un stimulateur cardiaque placé dans la poitrine du patient génère ces impulsions électriques qui sont transmises au cerveau, cela permettant une modulation réversible de ces zones en soulageant les symptômes moteurs tels que les dyskinésies, et l'amélioration des symptômes non moteurs.
Le DBS est devenu un traitement établi dans l’avancée de la maladie de Parkinson grâce à l'amélioration du fonctionnement moteur et des complications de la Lévodopa à long terme. "Tous les patients sélectionnés pour la DBS subissent des tests neuropsychologiques détaillés et une évaluation psychiatrique afin de définir les fonctions cognitives et les comorbidités psychiatriques potentielles, susceptibles de s’aggraver après une intervention chirurgicale», dit Krüger. La DBS améliore généralement les tremblements, mais aussi le ralentissement des mouvements et la rigidité musculaire accrue. Bien que largement utilisé pour les patients qui souffrent de la maladie de Parkinson depuis plus d'une décennie, une étude récente, avec la participation de l'équipe de Krüger a prouvé que la DBS peut déjà améliorer la qualité de vie dans les stades précoces de la maladie, où les fluctuations viennent juste de commencer.
Selon les auteurs, l'utilisation de l'un des traitements nécessite des informations précoces sur les patients ainsi qu’une communication précise entre les patients, les soignants et le neurologue traitant. Recommander les pompes à Apomorphine, le LCIG ou de la DBS est très individuel et doit être fait au cas par cas, après considérations des avantages et des inconvénients de chaque thérapie.
Publication originale:
"Advanced stages of PD: interventional therapies and related patient-centered care"
Rejko Krüger, Rüdiger Hilker, Christian Winkler, Michael Lorrain, Matthias Hahne, Christoph Redecker, Paul Lingor, Wolfgang H. Jost
Journal of Neuronal Transmission (2015), DOI: 10.1007/s00702-015-1418-0